Frecuentemente utilizo el antagonismo del bloqueo neuromuscular con neostigmina o sugammadex; preferentemente sugammadex ya que el bloqueador neuromuscular no despolarizante (BNMND) que uso casi siempre es rocuronio…
Tengo muy buena experiencia con neostigmina 30-60 mcg/kg 15 min antes de programar extubación, con un monitoreo cualitativo neuromuscular de TOF 2/4 como mínimo. Muy pocas ocasiones (1:20) tengo que reforzar el antagonismo de la neostigmina con sugammadex para tener TOF 4/4 y desvanecimiento tetánico negativo (estímulo tetánico sostenido).
Sugammadex es un antagonista de aminoesteroide (rocuronio, vecuronio) simplemente maravilloso: antagonismo inmediato, completo y sin los efectos secundarios de los anticolinesterásicos (sialorrea, bradicardia, arritmias, broncoespasmo, náuseas, alteraciones visuales…). En varios años utilizando sugammadex (¿7 años?) nunca he visto (ni lo creo, adelanto) un laringoespasmo inducido por sugammadex. Sí he presenciado y tratado múltiples laringoespasmos en 35 años de mi labor como anestesiólogo al extubar, al aspirar la cavidad orofaríngea, etc… Incluso, he visto más laringoespasmos por neostigmina (por la sialorrea) que por sugammadex. Pero, muy importante, tanto uno como otro NO son fármacos que por sí mismos induzcan espasmo laríngeo. No conozco un solo artículo que compruebe fiablemente que inducen laringoespasmo per se.
Todo paciente con parcial bloqueo neuromuscular o sin él, con anestesia superficial o consciente, podrá presentar laringoespasmo al manipular la cavidad orofaríngea, mover la cabeza, extubar… Pero no, por favor, culpar ni a la neostigmina ni al sugammadex.
Si fuera una tesis real que el sugammadex induce laringoespasmo, la FDA ya hubiera proscrito el uso del antagonista.
¿Por qué solo se señala al sugammadex si la neostigmina también antagoniza el bloqueo neuromuscular? De hecho, y como ya lo mencioné anteriormente, he visto más laringoespasmos por la salivación generada por la neostigmina. Pero, insisto, es la sialorrea, no culpo a la neostigmina.
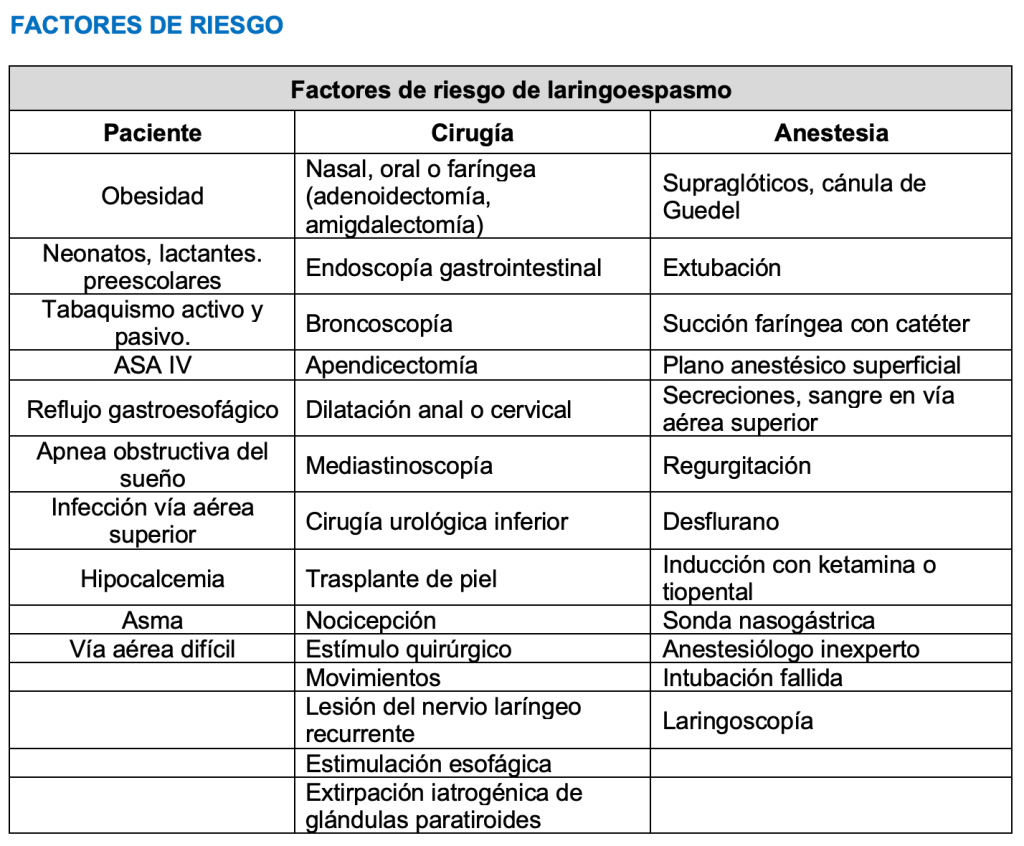
La manipulación de la vía aérea es la causa más frecuente de laringoespasmo, principalmente durante la intubación y extubación; el realizar laringoscopía con el paciente sedado o anestesiado sin bloqueo neuromuscular, el uso de mascarilla laríngea o cualquier dispositivo supraglótico, mascarilla facial, cánula nasofaríngea, cánula orofaríngea, cánulas orofaríngeas con manguito (COPA, Cuffed Oropharyngeal Airway), cánula de succión; presencia de sangre o secreciones, cuerpo extraño, endoscopía gastrointestinal, broncoscopía, colocación de sonda nasogástrica, gases fríos y secos, residuo de agua en las mangueras, polvo procedente de la cal sodada o baritada, cambio de posición y medicamentos administrados por vía nasal.
Las causas del laringoespasmo pueden ser mecánicas, químicas o térmicas en la zona glótica, estimulando las fibras aferentes de la rama interna del nervio laríngeo superior. Los receptores se distribuyen a lo largo de la glotis y la mayoría se encuentra en la superficie laríngea de la epiglotis.La inervación de la región supraglótica es por el nervio laríngeo superior, mientras que debajo de las cuerdas vocales es por el nervio laríngeo recurrente. Convergen en el núcleo del tracto solitario del bulbo raquídeo, lo que desempeña un papel esencial en la génesis de los reflejos de las vías aéreas superiores.
A continuación algunos artículos de interés:
1. Did sugammadex cause, or reveal, laryngospasm? N Chrimes. Anaesthesia. 2016 Sep;71(9):1112. Me pregunto si el laringespasmo descrito en el informe del caso de McGuire y Dalton no fue causado por Sugammadex, sino más bien al instrumentar la vía aérea a una profundidad insuficiente de anestesia [Anaesthesia 2016;71:487-92]? A partir de la descripción de la técnica proporcionada, parece que la maniobra de Bailey se realizó a una profundidad de anestesia de mantenimiento de 0.7 CAM. Con frecuencia, utilizo la maniobra de Bailey, y no sería de sorprender que aparezca un laringoespasmo en este plano de anestesia en un paciente con tono muscular ya normalizado. La presencia del bloqueo neuromuscular profundo no altera la estimulación de la vía aérea producida por esta maniobra, simplemente oculta las consecuencias motoras de esta estimulación hasta que el tono muscular normal se ha restaurado por el antagonismo del sugammadex, lo que permite que los impulsos de los nervios eferentes crucen la unión neuromuscular y provoquen la aducción de las cuerdas vocales y obstrucción. Es razonable esperar también una respuesta idéntica si se restauró el tono muscular normal antagonizando con neostigmina. El problema aquí parece derivarse de una errónea interpretación de las directrices de la Difficult Airway Society para la extubación [Anaesthesia 2012;67:318-40], que afirman que «ya sea bajo anestesia profunda o bloqueo neuromuscular es importante» para evitar la estimulación de las vías respiratorias durante la maniobra de Bailey, cuando el bloqueo neuromuscular debería ser considerado un complemento en lugar de una alternativa a la anestesia profunda. Sin anestesia profunda, la aferencia sensitiva y motora del arco reflejo que promueve el laringespasmo se producirá y revelará en toda forma al devolver el tono muscular normal por antagonismo del bloqueo neuromuscular.
La profundidad de anestesia requerida para prevenir la estimulación de los reflejos laríngeos en la extubación es similar a la requerida para colocar de manera segura un dispositivo de vía aérea supraglótico en la inducción, y es probable también que deba ser mayor una profundidad de la anestesia utilizando 0.7 CAM de agente volátil. En mi práctica lo que hago es administrar un bolo de propofol antes de realizar la maniobra de Bailey, rocíó las cuerdas vocales con lidocaína 10% y posiciono de manera óptima, en el supuesto caso de que tenga que colocar nuevamente el supraglótico. No retiro el tubo traqueal hasta que el supraglótico esté correctamente posicionado; no realizo la maniobra de Bailey en pacientes en los que sospecho no es adecuada la colocación del supraglótico. Insuflar los pulmones antes de desinflar el manguito de tubo traqueal, y confirmar el O2 y gas espirado a través del supraglótico, proporciona mayor seguridad (no una garantía) que el supraglótico está correctamente posicionado y funcionará como una vía aérea patente al retirar el tubo traqueal. Resumiendo, colocar un supraglótico al final de un caso con la maniobra de Bailey requiere las mismas condiciones, preparación y consideraciones, como si fuera a colocarse por primera vez en la inducción de la anestesia.
2. Postoperative negative pressure pulmonary edema following repetitive laryngospasm even after reversal of neuromuscular blockade by sugammadex: a case report. Ji Hyeon Lee. Korean J Anesthesiol. 2017 Feb;70(1):95-99. El laringoespasmo, una oclusión de la glotis, puede ocurrir en cualquier momento durante la anestesia y se asocia con complicaciones perioperatorias graves como hipoxia, hipercabia, aspiración, broncoespasmo, arritmia, edema pulmonar por presión negativa, una recuperación más prolongada, paro cardíaco y, finalmente, muerte. Es importante destacar que el edema pulmonar por presión negativa (EPPN) es una rara complicación potencialmente mortal, pero bien descrita, relacionada con la obstrucción aguda y crónica de las vías respiratorias superiores. El sugammadex, que disminuye las complicaciones pulmonares posoperatorias por bloqueo neuromuscular residual, puede tener un papel indirecto en el desencadenamiento de la presión intratorácica negativa al aumentar la fuerza de los músculos respiratorios de forma rápida y eficaz en la obstrucción aguda de las vías respiratorias superiores. Laringoespasmo no inducido directamente por sugammadex, sino por plano anestésico superficial, secreciones orales, estímulo al retirar el tubo endotraqueal… Informamos un caso de EPPN posoperatorio después de un laringoespasmo después de antagonizar con sugammadex el bloqueo neuromuscular por rocuronio.
3. Sugammadex and laryngospasm. Tsai-Shan Wu. J Clin Anesth. 2019 Sep;56:52. Did sugammadex cause or reveal laryngospasm? La respuesta aún se desconoce [Anaesthesia 2016;71:487-92]. Compartimos un caso que presentó laringoespasmo inducido (?) por sugammadex. Varón de 66 años, 163 cm de estatura y 65 kg de peso (IMC 24.5). Colostomía urgente por cáncer. Clasificado como estado físico III de la ASA por ser fumador crónico, hipertenso, fibrilación auricular y enfermedad pulmonar obstructiva crónica. Mantuvo su medicación y seguimiento regulares. Inducción de la anestesia general con propofol e infusión de remifentanilo, lidocaína 2% 40 mg y rocuronio 50 mg, intubación sin eventualidad alguna. Cirugía sin complicación alguna con una duración de 50 min. La infusión continua de propofol y remifentanilo se interrumpió al finalizar el procedimiento. Cuando el paciente pudo respirar espontáneamente, se le administró neostigmina 3 mg y glicopirdato 1 mg. Una vez que el volumen corriente alcanzó los 350 mL, se retiró el tubo traqueal. El paciente nos indica que respira con dificultad. Se administra sugammadex 100 mg por vía intravenosa. Un minuto después de la administración de sugammadex, el paciente señaló su boca y mencionó que no podía hablar, con respiración restrictiva y estridor. Se realizó maniobra de empuje mandibular, ventilación con máscara facial con O2 100% con presión positiva continua de 30 cmH2O por sospecha de laringoespasmo. Sin embargo, todavía no podía ventilar y no podía oxigenar. Un minuto después, su frecuencia cardíaca llegó a 45 lpm y se presentó cianosis. Se intentó la videointubación de emergencia, pero fracasó por no poderse visualizar las cuerdas vocales. La laringoscopía directa reveló laringoespasmo completo. Tras la intubación, la capnografía mostró una EtCO2 79 mmHg y el paciente despertó 1 min después de la hiperventilación. Tres minutos después, se retiró el tubo endotraqueal y se envió al paciente a la unidad de cuidados postanestésicos. Una hora más tarde, fue enviado a la sala general con signos vitales estables.
Nuestro caso confirma, más 8 informes anteriores, pacientes que experimentaron obstrucción transitoria de las vías respiratorias superiores (laringoespasmo) después de la administración de sugammadex en pacientes ya extubados [Anaesthesia 2017;72:412-3], lo que Dalton relacionó con el retorno rápido y completo del tono muscular a partir de un bloqueo neuromuscular profundo, en paciente inconsciente sin tubo traqueal [Anaesthesia 2017;72:545-6]. Sin embargo, nuestro caso fue diferente de los informes anteriores, bloqueo neuromuscular profundo versus ligero y paciente inconsciente versus despierto. Además, nuestro paciente tenía antecedentes de enfermedad pulmonar obstructiva crónica, apnea obstructiva del sueño, tabaquismo intenso, obesidad y clasificación ASA III, y un plano de anestesia ligero contribuiría a este escenario [Anaesth Analg 2017;23(Sl):S74-80].Concluyendo, los anestesiólogos deben tener en cuenta que puede presentarse laringoespasmo al administrar sugammadex en pacientes no intubados.
4. Incidence of negative-pressure pulmonary edema following sugammadex administration during anesthesia emergence: a pilot audit of 27,498 general anesthesia patients and literature review. Kao CL. J Clin Anesth 2020;62:109728. Sugammadex se ha comercializado en más de 40 países en todo el mundo y demuestra una rápida y completa reversión del bloqueo neuromuscular por rocuronio. Sin embargo, se han publicado casos de edema agudo pulmonar por presión negativa (EAPPN) en la emergencia de la anestesia cuando se utilizó sugammadex [Acute Crit Care 2018;33:191-5]. El presente estudio diseñó para examinar este problema. La población de estudio comprendió pacientes quirúrgicos que recibieron intubación traqueal o vía aérea con mascarilla laríngea (ML) como parte de la anestesia general. Se excluyeron a los pacientes que ingresaron en la unidad de cuidados intensivos después de la cirugía. El objetivo fue comparar la incidencia de EAPPN en pacientes que recibieron sugammadex con aquellos que no recibieron sugammadex durante en la emergencia de la anestesia; en consecuencia, los sujetos se dividieron en dos grupos (grupo sugammadex y grupo No sugammadex).
Los criterios para el diagnóstico de EAPPN incluyeron examen físico (p. ej., sibilancias y estertores inspiratorios gruesos) y hallazgos en radiografía de tórax. El resultado primario fue la diferencia en la incidencia de EAPPN con o sin la administración de sugammadex durante la emergencia de la anestesia. La significancia estadística fue indicada por p < 0.05.
27,498 pacientes sometidos a anestesia general desde enero de 2018 a diciembre de 2019 (grupo sugammadex, n = 2164 y grupo No sugammadex, n = 25,334). Se identificaron 2 pacientes con EAPPN en el postoperatorio. Paciente 1, varón 46 años, ASA II, 68 kg y 177 cm, IMC 21.7 kg/m2), antecedentes de asma y cirugía endoscópica de senos nasales. Paciente 2, mujer 29, ASA I, 62 kg y 164 cm, IMC 23.1 kg/m2), cirugía nasal. En ambos pacientes, la radiografía de tórax preoperatoria no fue destacable. Paciente 1, laringoespasmo tras la administración de sugammadex y extubación en plano profundo; la ventilación con mascarilla facial fue difícil persistiendo varios minutos postlaringoespasmo. Paciente 2, obstrucción aguda de la vía aérea superior mientras el paciente mordía el tubo traqueal en la emergencia de la anestesia general después de la administración de sugammadex. En ambos pacientes se diagnosticó EAPPN en la unidad de cuidados postanestésicos y la disnea desapareció 24 horas después de un tratamiento conservador. La incidencia de EAPPN fue del 0.09% en el grupo de Sugammadex y del 0% en el grupo de No sugammadex (p = 0.0004; odds ratio 58.6).
La EAPPN generalmente es causada por la obstrucción de las vías respiratorias superiores combinada con un rápido aumento de la fuerza de los músculos respiratorios (inspiratorios), lo que conduce a una presión intratorácica fuertemente negativa que provoca el edema pulmonar. En este estudio, encontramos que el uso de sugammadex aumentó significativamente el riesgo de EAPPN en comparación con los pacientes en los que no se utilizó este agente de reversión. Varios estudios de casos informaron que la EAPPN puede ser causada por un aumento inducido por sugammadex en la fuerza de los músculos respiratorios inspiratorios una vez que se produjo la obstrucción de las vías respiratorias superiores o la rigidez muscular. Hasta donde sabemos, nuestro informe es el primero en aclarar si el uso de sugammadex aumentó el riesgo de EAPPN en la práctica clínica.
El presente estudio tiene varias limitaciones:
– Primero, recopilamos datos de la base de datos de facturación de anestesia; por lo tanto, las características físicas de los pacientes, comorbilidades, detalles quirúrgicos y número de pacientes que recibieron neostigmina como agente de reversión no estaban disponibles. La identificación precisa de estos datos reduciría el sesgo del estudio.
– Segundo, los otros factores de riesgo de EAPPN no se evaluaron debido al número limitado de pacientes.
– Tercero, la EAPPN sigue siendo una complicación poco común después de la administración de anestesia general. Nuestro estudio puede tener poca fiabilidad para detectar la diferencia deseada debido a un tamaño de muestra más pequeño.
– Cuarto, los casos notificados de EAPPN asociados a sugammadex eran todos de la población asiática según la revisión de la literatura. Por lo tanto, nuestros resultados pueden no generalizarse a poblaciones no asiáticas. Se necesitan más estudios para abordar este problema.
En conclusión, este estudio piloto mostró que el uso de sugammadex podría ser un factor de riesgo significativo para la EAPPN en pacientes anestesiados si la obstrucción aguda de las vías respiratorias ocurriera de manera inesperada. Nuestros hallazgos pueden permitir a los anestesiólogos desarrollar una guía de práctica clínica para el uso de sugammadex. Se deben realizar más estudios a gran escala para respaldar nuestros hallazgos.

Sugammadex and negative pressure pulmonary edema: what you see is not what you get. Sorin J Brull. Journal of Clinical Anesthesia 67 (2020) 109971. Leímos con interés la carta de Kao [J Clin Anesth. 2020 Jun;62:109728], en donde informa sobre 2 pacientes que presentaron edema agudo pulmonar por presión negativa (EAPPN) después del antagonismo del bloqueo neuromuscular con sugammadex. Estos informes podrían ser muy importantes para la seguridad del paciente, ya que alertan a los médicos sobre efectos secundarios infrecuentes pero significativos. Al mismo tiempo, creemos que estos informes deben proporcionar la interpretación más probable y correcta de los hechos y, por lo tanto, proporcionamos varios comentarios sobre dicho estudio.
– Primero, el título es engañoso, ya que los autores afirman informar la incidencia de EAPPN «después de la administración de sugammadex …» De hecho, los 2 casos de EAPPN ocurrieron entre 2,164 pacientes que recibieron sugammadex, no los 27,498 «pacientes con anestesia general», que incluyó a 25,334 pacientes «no sugammadex”.
– Segundo, «el laringoespasmo se produjo después de la administración de sugammadex y la extubación profunda». El hecho de que el paciente sea capaz de responder al estímulo de la extubación traqueal con laringoespasmo demuestra que, de hecho, la extubación ocurrió durante una profundidad anestésica inadecuada; sin embargo, la recuperación del paciente del bloqueo neuromuscular fue totalmente suficiente para permitir que ocurriera la respuesta fisiológica normal (laringoespasmo) con esfuerzos inspiratorios intensos. Esta «complicación» es más probable que sea un error clínico en el manejo de la emergencia, del despertar de la anestesia general, que el resultado de la administración de sugammadex.
– Tercero, lo mismo puede decirse del otro paciente, que «mordió el tubo traqueal durante la recuperación de la anestesia general después de la administración de sugammadex». La oportunidad de la paciente de manifestar “presión intratorácica fuertemente negativa que causa edema pulmonar” se debió al hecho de que la paciente no tenía un bloque de mordida insertado adecuadamente antes de salir de la anestesia, lo que le permitió morder el tubo traqueal, ocluyendo durante fuertes esfuerzos inspiratorios que provocaron la presión negativa intrapulmonar. Esta complicación difícilmente puede atribuirse a la administración de sugammadex. Por lo tanto, este trabajo piloto es engañoso al afirmar que es «la primera en aclarar si el uso de sugammadex aumentó el riesgo de EAPPN en la práctica clínica».
– Cuarto, aunque aplaudimos los esfuerzos de Kao para caracterizar aún más los matices clínicos del uso de sugammadex, advertimos a otros sobre los errores en identificar la causa más probable, verdadera, del laringoespasmo de los dos pacientes presentados y relacionados con una importante complicación perioperatoria al despertar de la anestesia general.

Ahora que has leído y analizado la publicación te invitamos a participar enviándonos tu opinión en el campo de texto inferior. ¡Gracias!
